Жидкое состояние вещества
1. Жидкость и пар как равновесная система
Из уравнения Ван-дер-Ваальса в применении к реальным газам следует, что при известных значениях температуры, давления и величин а и b газ образует систему из жидкости и газа (пара). До сих пор нет законченной теории жидкости, и потому мы рассмотрим систему жидкость — пар только с точки зрения учения о физическом равновесии.
Представим себе сосуд (рис. 1), закрытый поршнем, к которому приложен груз P. Часть сосуда наполнена жидкостью, остальная часть — паром. Каждой данной температуре соответствует определенная концентрация пара C. Концентрацию будем выражать числом молекул (атомов) в единице объема.
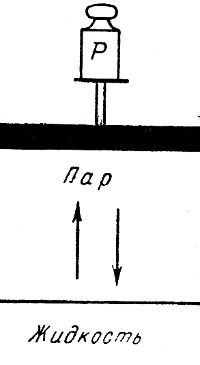
Рис. 1. Равновесная система из жидкости и ее пара
Так как давление пара на стенки сосуда прямо пропорционально концентрации пара, то обыкновенно концентрацию заменяют пропорциональной ей величиной — давлением пара. При каждой данной температуре мы имеем так называемое подвижное равновесие. Предполагается, что в каждый данный момент столько жидкости переходит в состояние пара, сколько пара переходит в состояние жидкости.
Скорость процесса испарения прямо пропорциональна концентрации жидкости, скорость процесса конденсации прямо пропорциональна концентрации пара. Закон этот называется законом концентраций или, если речь идет о химическом равновесии, — законом активных или действующих масс.
Он выражается математически так:
Vиспар = K · cжидк; Vконд = K' · cпар,
где K и K' суть постоянные величины. В случае равновесия Vиспар = Vконд
K · сжидк = K' · cпар.
Так как вследствие испарения концентрация жидкости не меняется, остается постоянной, то cжидк есть величина постоянная. Перенеся в уравнении постоянные величины в одну сторону, переменные в другую, получим:
cпар = Const.
Или, заменив концентрацию пара пропорциональной ей величиной давления пара, получим:
Pпар = Const,
т.е. каждой данной температуре соответствует определенная концентрация или определенное давление пара. Пар, находящийся в равновесии с жидкостью, называется насыщенным паром.
Если, не изменяя температуры, мы сдвинем поршень вниз, концентрация пара увеличится, а следовательно, скорость конденсации станет больше скорости испарения, и через измеримый промежуток времени часть пара перейдет в жидкость. Это будет продолжаться до тех пор, пока концентрация пара не уменьшится до первоначальной величины, тогда опять наступит равновесие.
Если сдвинуть поршень вверх, то уменьшится концентрация пара и скорость конденсации, перевес возьмет скорость испарения жидкости, в результате чего концентрация пара начнет возрастать. Это будет продолжаться, пока концентрация пара не увеличится до первоначальной величины.
Если температура возрастает, то, как правило, для всех жидкостей концентрация пара (а следовательно, и давление) в равновесной системе растет. Обычно этот закон выражается так: давление насыщенного пара жидкости растет с температурой.
На рис. 2 приведена кривая возрастания давления насыщенного пара воды с изменением температуры.
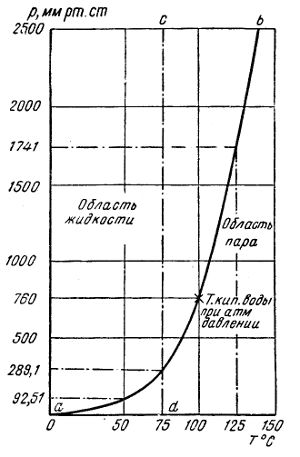
Рис. 2. Кривая давления насыщенного пара воды при 0—150°C
На диаграмме приводится давление насыщенного пара воды при температурах 0—150°C. Например, при 50°C давление насыщенного пара равно 92,51 мм рт.ст., при 100°C 760 мм рт.ст., при 125°C 1741 мм рт.ст. и т.д.
Кривая давления насыщенного пара делит плоскость диаграммы на две области: область жидкости и пара; вдоль линии ab имеет место равновесие между паром и жидкостью.
На прямой dc, отвечающей температуре 75°C, только при давлении 289,1 мм рт.ст. будем иметь равновесную систему пар—жидкость (точка, лежащая на кривой ab). Все точки, соответствующие ординатам 290—2500 мм рт.ст., отвечают жидкой воде. Это значит, что каждая точка, определяемая своей абсциссой температуры и ординатой давления в области жидкости, соответствует воде в состоянии жидкости; каждая точка в области пара — ненасыщенному пару воды; каждая точка на линии ab — системе из жидкости и пара.
Например, из диаграммы следует, что при 50°C и давлении 10 мм рт.ст. вода находится в состоянии ненасыщенного пара, при той же температуре и давлении 500 мм рт.ст. — в состоянии жидкости; при 50° и при давлении 92,51 мм рт.ст. мы имеем равновесную систему из жидкой воды и ее насыщенного пара.
Температура кипения жидкости. Температурой кипения жидкости называется температура, при которой давление ее насыщенного пара равно внешнему давлению.
Например, из диаграммы следует, что давление насыщенного пара воды при температуре 75°C равно 289,1 мм рт.ст. Это значит, что 75°C и есть температура кипения воды при внешнем давлении на жидкость 289,1 мм рт.ст.
Давление насыщенного пара воды при температуре 100°C равно 760 мм рт.ст.; 100°C и есть температура кипения воды при внешнем давлении 760 мм рт.ст.
Давление насыщенного пара воды при температуре 125°C есть 1741 мм рт.ст. Следовательно, температура кипения воды при данном давлении равна 125°C.
Итак, температура кипения зависит от внешнего (атмосферного) давления на жидкость.
Обычно температура кипения жидкости дается при атмосферном давлении. За атмосферное давление условно принимают давление в 760 мм рт.ст. на см2.
2. Равновесная система твердое вещество — пар
Вещество в твердом состоянии также дает пар, который с твердым веществом составляет равновесную систему такого же рода, как равновесная система жидкость — пар.
Процесс перехода твердого вещества в пар без предварительного перехода в жидкое состояние называется улетучиванием, сублимированием, или возгонкой.
Как и в случае системы жидкость — пар, мы можем построить диаграмму твердое вещество — пар и на этой диаграмме мы будем также иметь две области: область пара и область твердого вещества, которые разделяются кривой.
3. Твердое вещество — жидкость как равновесная система
Вещество в кристаллическом и в жидком состоянии составляет также равновесную систему, которая определяется, как и в двух предыдущих случаях, двумя параметрами — температурой и давлением.
4. Диаграмма физического состояния
Соединив вместе три диаграммы пар — жидкость, твердое вещество — пар и твердое вещество — жидкость, получим так называемую диаграмму физического состояния данного вещества. На рис. 3 приведена такая диаграмма для воды. По оси абсцисс отложены температуры в градусах Цельсия, по оси ординат — логарифмы давлений в атмосферах.
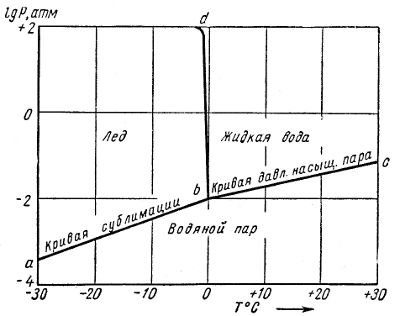
Рис. 3. Диаграмма состояния воды
На диаграмме рис. 3 видны области температур и давлений, в которых вода может быть только в жидком состоянии, в состоянии льда и в состоянии пара. Области эти делятся линиями ab, bc и bd, на которых отмечаются те давления и температуры, когда одновременно существуют равновесные системы: пар — лед (ab), пар — жидкость (bc), лед — жидкость (bd). Иначе: кривая ab есть кривая давлений сублимации, bc — кривая давлений насыщенного пара, bd — кривая температур плавления в зависимости от давления.
На диаграмме есть одна точка, соответствующая температуре +0,0075°C и давлению 4,6 мм рт.ст., в ней одновременно существуют лед, пар и вода. Эта точка называется тройной точкой.
