Проницаемость клеток для неэлектролитов
Изучение проницаемости клеток для неэлектролитов сыграло важную роль в выяснении закономерностей прохождения веществ через клеточную мембрану, ее состава, строения и физико-химических свойств.
Исследования Е. Овертона (1902) и позднее Р. Колландера и X. Берлюнда (1933, 1954), результаты которых подтверждены И.М. Даймондом и Е.М. Райтон (1969), показали, что скорость проникновения в клетки широкого круга неэлектролитов определяется их гидрофобностью: чем гидрофобность выше, тем больше скорость их проникновения в клетку. Эти результаты являются одним из важнейших аргументов, доказывающих наличие на поверхности клеток барьера липидной природы.
Однако такие неэлектролиты, как мочевина и ее производные, амиды, этиленгликоль, глицерин и другие спирты, обладающие резко выраженными гидрофильными свойствами, как правило, с большой скоростью проникают в клетки, так же как и молекулы воды. Эти данные привели к выводу, что липидная мембрана имеет поры, или гидрофильные участки, молекулярного размера (0,8 нм), обеспечивающие диффузию в клетку гидрофильных неэлектролитов. Чем меньше размер молекул этих веществ, тем они быстрее поступают в клетку. Гидрофильные неэлектролиты, радиус молекул которых больше 0,4 нм, практически не проникают в клетки, например полисахарид инулин. Известно, однако, что некоторые гидрофильные неэлектролиты, имеющие такую же величину молекул, все-таки поступают в клетки. Теперь доказано, что в этом случае действует специфическая транспортная система, обеспечивающая перенос неэлектролитов через мембрану.
Наиболее полно из всех неэлектролитов изучена транспортная система сахаров. В эпителиальных клетках кишечника и почечных канальцах транспорт некоторых сахаров является активным, так как совершается против градиента концентрации и требует затраты энергии. Поступление сахаров в клетки из просвета кишечника (всасывание) и почечных канальцев (реабсорбция) совершается через апикальную мембрану, выход сахаров из этих клеток в лимфу и кровь протекает пассивно по градиенту концентрации через базальную и латеральные мембраны (рис. 18). Имеются данные, свидетельствующие о взаимной связи потоков сахара и натрия в этих клетках, на основании чего полагают, что энергия натриевого градиента используется для активного транспорта сахара (сахар транспортируется вместе с Na+, поступающим в клетку по градиенту концентрации). Ингибиторы обмена подавляют активный транспорт сахара внутрь этих клеток.
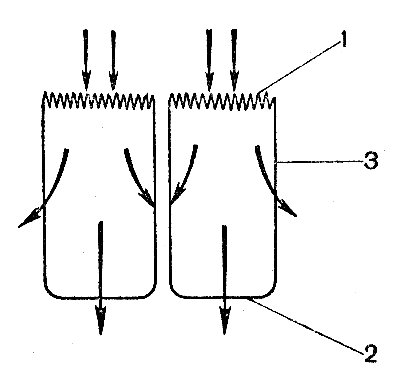
Рис. 18. Потоки сахара в эпителиальных клетках кишечника через мембраны: 1 — апикальную; 2 — базальную; 3 — латеральную.
В эритроцитах, жировых, нервных и мышечных клетках транспорт сахаров является пассивным, так как происходит по градиенту концентрации и идет до тех пор, пока концентрации сахара в воде среды и клетки не выровняются (с учетом более низкой растворимости сахара в воде протоплазмы).
Веским доказательством наличия транспортной системы для сахаров служит тот факт, что поступление углеводов в клетки подчиняется правилу Михаэлиса — Ментен — с повышением концентрации сахара в среде начальный поток его внутрь (Vin) возрастает по прямо пропорционально, а стремится к пределу. Этот процесс подчиняется уравнению:
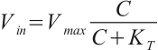
где С — концентрация сахара в среде; Vmax, KT — константы транспорта.
О наличии транспортной системы сахаров говорит также существование конкуренции между сахарами за поступление в клетку. В силу этого же возникает и явление так называемого противопотока сахара — при равновесном распределении одного сахара добавление в среду другого вызывает временный поток первого сахара из клетки в среду против градиента концентрации. Этот эффект возникает благодаря конкуренции за переносчики между двумя сахарами только с одной внешней стороны мембраны, что ведет к неравенству потоков первого сахара: поступление его внутрь клетки снижается, поток же наружу остается вначале без изменений.
Транспортная система большинства клеток специализирована для переноса глюкозы и близких ей по строению сахаров. Так, в мышечных волокнах она транспортирует следующие стереоизомеры пентоз и гексоз: D-глюкоза, D-галактоза, D-ксилоза, L-арабииоза, D-рибоза. Практически не проникают D-арабиноза, сахароза, раффиноза. Непроникающие сахара поступают лишь в так называемое тканевое или межклеточное пространство. Однако межклеточное пространство для этих сахаров больше инулинового. Это объясняется, видимо, тем, что для непроникающих сахаров доступно некоторое ограниченное пространство волокна, возможное в системе саркоплазматического ретикулума.
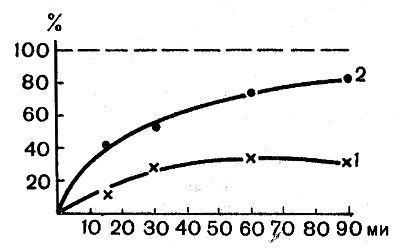
Рис. 19. Влияние инсулина на поступление D-ксилозы в мышечные подокна крысы (Corlin a Hechter, 1961): 1 — без инсулина; 2 — с инсулином. По оси абсцисс — время от начала помещения мышцы в раствор сахара, в минутах; по оси ординат — содержание сахара в мышце, и % от его количества в среде (0,4%), принятого за 100%
В присутствии инсулина скорость транспорта сахаров значительно выше, чем без него (рис. 19). Инсулин повышает скорость поступления в клетки только тех сахаров, которые и без него проникают в клетки, но медленно. Стимулирующий эффект инсулина проявляется при концентрации около 10 мкед/мл и достигает максимума при 1000 мкед/мл. Такой же стимулирующий эффект на транспорт сахаров в мышечные волокна, как и инсулин, оказывают ингибиторы энергетического обмена — динитрофенол, азид натрия, моноиодацетат (рис. 20). Это явление рассматривается как компенсаторная реакция клетки. Ингибиторы обмена подобно инсулину не влияют на распределение непроникающих сахаров между клеткой и средой.
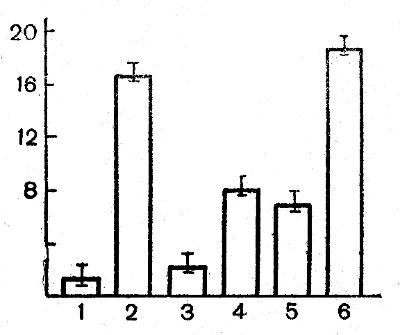
Рис. 20. Влияние ингибиторов обмена на поступление D-ксилозы в икроножные мышцы лягушки (Дорошенко, 1968). По оси ординат — внутриклеточная концентрация ксилозы, мМ; 1 — контроль; г — 2,4-динитрофенол (0,3 мМ); 3 — 2,4-динитрофенол (0,3 мМ) + флорицин (1 мМ); 4— азид натрия (16 мМ); 5 — моноиодоуксусная кислота (0,25 мМ); 6 — инсулин (0,5 ед/мл)
Повышение скорости транспорта сахаров наблюдается также при сокращении мышц, вызванном раздражением электрическим током (рис. 21), действием хлористого натрия и хлористого калия. Стимулирующий эффект этих факторов является, по-видимому, следствием повышения концентрации свободного кальция в миоплазме.
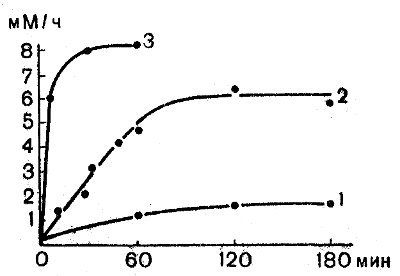
Рис. 21. Влияние частоты и длительности электрического раздражения на скорость транспорта 3-0-метилглюкозы в портняжной мышце лягушки (Holloszy a Narahara, 1965). По оси абсцисс — длительность раздражения, в минутах; по оси ординат — скорость транспорта 3-0-метилглюкозы, измеренная непосредственно после раздражения, мМ/ч. Частота раздражения: 1—3; 2—20; 3—120 имп/мин
Флоретин и флорицин (глюкозиды, содержащиеся в коре яблони, груши, вишни) обратимо тормозят транспорт через мембрану клеток всех проникающих сахаров. Они полностью снимают стимулирующий эффект инсулина и ингибиторов обмена (рис. 20). Полагают, что эти ингибиторы транспорта конкурируют с сахарами, блокируя их переносчики. Тормозят транспорт сахаров также тиоловые яды и наркотики. Но это торможение неспецифическое, и в его основе не лежит конкуренция.
Транспортная система для сахаров развивается на определенных стадиях эмбриогенеза. Так, мышечная ткань эмбрионального сердца цыпленка до седьмого дня развития одинаково проницаема для различных стереоизомеров сахаров и не чувствительна к инсулину. В скелетных мышцах чувствительность к инсулину возникает в эмбриогенезе еще позднее.
Биологическое значение формирования специфических транспортных систем в клетках состоит, вероятно, в обеспечении тонкой регуляции проницаемости клеток, которая вряд ли могла быть достигнута путем растворимости веществ в мембране или их прохождения через водные поры мембраны.
В разных клетках скорости утилизации сахара различны. Так, в мышечных волокнах скорость фосфорилирования выше, чем скорость транспорта. Поэтому в условиях равновесия глюкозы в мышечных клетках содержится меньше, чем в среде (Q < 1). Обратное соотношение наблюдается в эритроцитах человека и в клетках печени, так как поступление глюкозы происходит с большей скоростью, чем ее утилизация. В связи с этим концентрация глюкозы в этих клетках в стационарных условиях равна ее концентрации в плазме крови (Q = 1). В таблице 5 показано распределение глюкозы в норме у животных и человека. Видно, что величина коэффициента распределения у различных организмов сильно варьирует.
| Таблица 5. Распределение глюкозы между эритроцитами и сывороткой у некоторых видов животных и у человека (Somogyi, 1933) | |
| Объект исследования | Q = Cкл/Cср |
| Бык | 0,18 |
| Теленок | 0,36 |
| Лошадь | — |
| Баран | 0,16 |
| Собака | 0,23 |
| Кошка | 0,28 |
| Кролик | 0,29 |
| Морская свинка | 0,33 |
| Обезьяна | 0,82 |
| Человек | 0,80 |
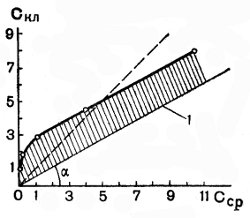
Рис. 22. Зависимость содержания лактозы в дрожжах (Скл) от концентрации ее в окружающей равновесной жидкости (Сср)
Коэффициент распределения зависит также от количества сахара в среде. При малых концентрациях сахара в среде его концентрация в клетках больше, а при больших, наоборот, в клетках меньше, чем в среде. Это хорошо видно на рисунке 22, где представлена зависимость концентрации лактозы в винных дрожжах от концентрации ее в среде. Этот сахар винными дрожжами не сбраживается. Представленная кривая может быть разложена на две компоненты. Прямолинейная компонента (1) отражает зависимость концентрации растворенного сахара в клетке (С) от концентрации его в среде (Сср) и подчиняется закону распределения Генри:
C = K · Cср ,
где K — коэффициент Генри и равен он tg α. В данном случае К = = 0,55, т.е. растворимость в воде дрожжевых клеток на 45% ниже, чем в среде.
Вторая компонента (заштрихованная область) соответствует количеству адсорбированного сахара (А). Зависимость его от концентрации в среде описывается изотермой адсорбции, подчиняющейся уравнению Лангмюра:
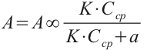
где А∞ — предел адсорбции (он равен отрезку ординаты, отсекаемому продолжением прямой) и a — константа крутизны нарастания изотермы (она равна концентрации сахара в среде, при которой количество адсорбированного неэлектролита равно 0,5 А ∞.
Суммарная концентрация сахара в клетке будет подчиняться уравнению:
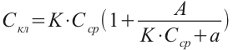
Зависимость величины коэффициента распределения лактозы (Q) от концентрации ее в среде представлена на рисунке 23.
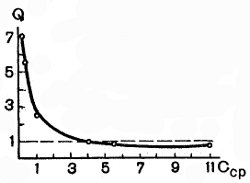
Рис. 23. Зависимость коэффициента Q от концентрации лактозы в окружающей равновесной жидкости (Сср, %) при распределении лактозы между дрожжами и окружающей средой
Таким образом, при больших концентрациях сахара в среде содержание его в клетке обусловлено в основном пониженной растворимостью в воде протоплазмы, а при малых концентрациях на первое место выступает адсорбция (поглощение), которая может обеспечить значительный перевес в содержании неэлектролита в клетке над содержанием в окружающей жидкости.
Микроорганизмы обладают способностью аккумулировать проникающие сахара из растворов с очень низкой их концентрацией, так что коэффициент распределения сахара (Q) может достигать десятков тысяч. Это объясняется, видимо, тем, что в мембранах бактерий Имеются специфические белки, обладающие большим родством к сахарам, так называемые транспортные белки. Однако не все сахара и не всеми микроорганизмами могут транспортироваться против градиента концентрации. В некоторых случаях наблюдается пассивный транспорт или полное отсутствие транспорта внутри клеток. Транспортная система микроорганизмов для сахаров обладает строгой специфичностью.
